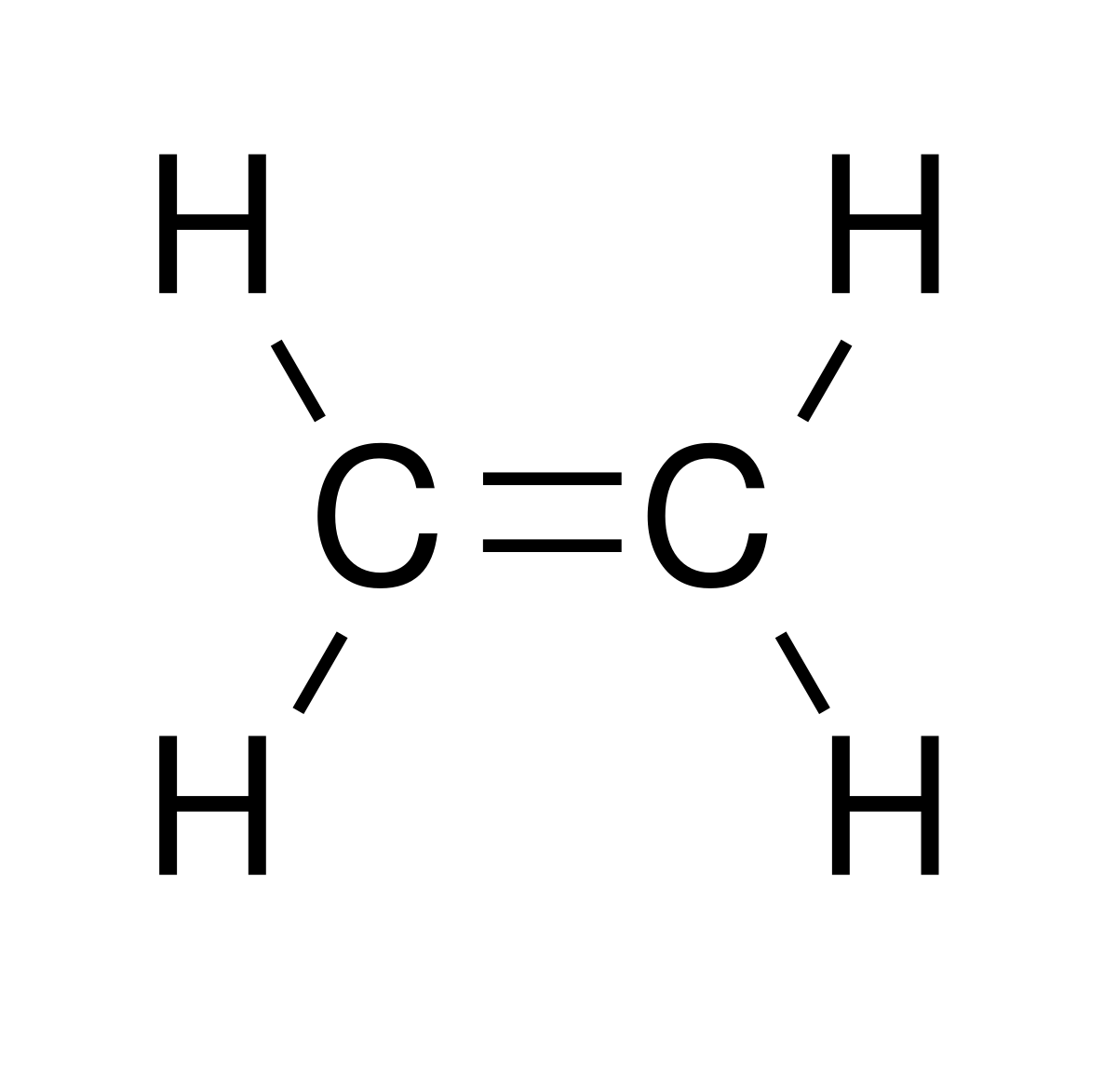
Ethylene, còn được gọi theo danh pháp IUPAC là Ethene, là một hydrocarbon không no đơn giản nhất thuộc dãy anken.
Giới thiệu chung
Ethylene, còn được gọi theo danh pháp IUPAC là Ethene, là một hydrocarbon không no đơn giản nhất thuộc dãy anken.

- Tên gọi:
- Tên IUPAC: Ethene
- Tên thường gọi: Ethylene
- Công thức hóa học: C₂H₄ hoặc H₂C=CH₂
- Khối lượng phân tử: 28.054 g/mol
- Mô tả tổng quan: Ethylene là một hợp chất hữu cơ không no với một liên kết đôi carbon-carbon. Ở điều kiện tiêu chuẩn, nó là một chất khí không màu, dễ cháy, có mùi ngọt nhẹ và xạ hương khi tinh khiết.
Tính chất lý hóa
Tính chất vật lý
- Trạng thái: Khí không màu ở nhiệt độ và áp suất phòng.
- Màu sắc: Không màu.
- Mùi vị: Mùi ngọt nhẹ và xạ hương khi tinh khiết.
- Độ tan: Ít tan trong nước (131 mg/L ở 25 °C), tan tốt trong các dung môi không phân cực.
- Nhiệt độ nóng chảy: -169.2 °C.
- Nhiệt độ sôi: -103.7 °C.
- Tỷ trọng: 1.178 kg/m³ ở 15 °C (dạng khí), nhẹ hơn không khí.
- Tính phân cực: Phân tử không phân cực do sự phân bố điện tích đối xứng.
- Tính dễ cháy: Rất dễ cháy và có thể tạo hỗn hợp nổ với không khí.
Tính chất hóa học
- Tính chất đặc trưng: Liên kết đôi carbon-carbon (C=C) là trung tâm phản ứng của ethylene, khiến nó dễ dàng tham gia vào các phản ứng cộng. Liên kết π trong phân tử ethylene là vùng có mật độ electron cao, do đó nó dễ bị tấn công bởi các tác nhân electrophin.
- Phản ứng cháy: Ethylene cháy hoàn toàn trong oxy tạo thành carbon dioxide và nước, đây là một phản ứng tỏa nhiệt mạnh. C₂H₄ + 3O₂ → 2CO₂ + 2H₂O
- Phản ứng cộng (Addition reactions):
- Cộng halogen: Ethylene phản ứng với halogen (ví dụ: Br₂, Cl₂) để tạo thành dihaloankan. C₂H₄ + X₂ → C₂H₄X₂ (với X = Cl hoặc Br)
- Cộng hydro (Hydro hóa): Ethylene có thể trải qua phản ứng hydro hóa với hydro (H₂) khi có mặt xúc tác kim loại như niken (Ni), palađi (Pd) hoặc platin (Pt) để tạo thành etan. C₂H₄ + H₂ → C₂H₆ (xúc tác Ni/Pd/Pt)
- Cộng hydro halogenua (HX): Ethylene phản ứng với các hydro halogenua (ví dụ: HBr) để tạo thành haloankan. H₂C=CH₂ + HBr → CH₃CH₂Br
- Cộng nước (Hydrat hóa): Ethylene có thể được hydrat hóa trực tiếp với nước để tạo thành etanol, thường được xúc tác bởi axit. C₂H₄ + H₂O → CH₃CH₂OH
- Phản ứng trùng hợp (Polymerization): Ethylene có khả năng trùng hợp để tạo thành polyetylen, một loại nhựa được sử dụng rộng rãi. n(C₂H₄) → [-CH₂-CH₂-]n