Giới thiệu chung
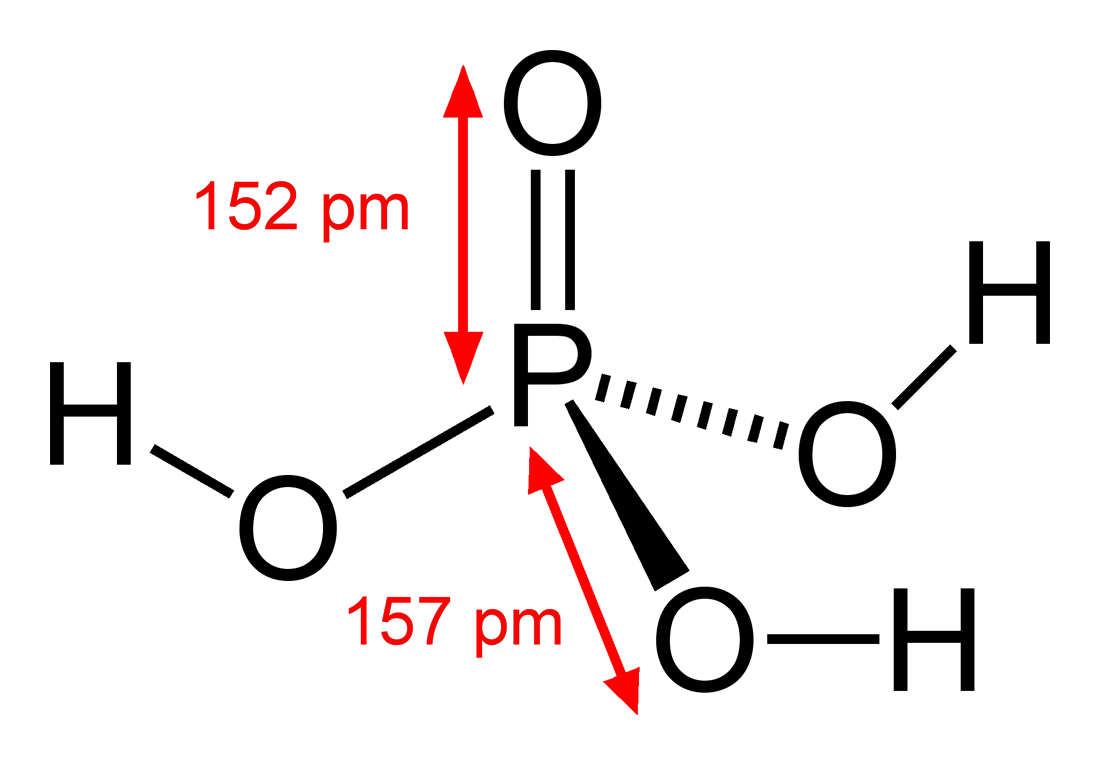
Axit phosphoric, còn được biết đến với tên gọi axit orthophosphoric, là một axit vô cơ có công thức hóa học là H₃PO₄. Nó có khối lượng phân tử khoảng 97.994 g/mol. Ở dạng tinh khiết, axit phosphoric là một chất rắn tinh thể không màu, không mùi. Tuy nhiên, trong thương mại và ứng dụng thực tế, nó thường được biết đến nhiều nhất ở dạng dung dịch lỏng, sánh, trong suốt và không màu, thường có nồng độ 85%. Axit phosphoric là một axit ba nấc (triprotic acid) có độ mạnh trung bình.
Tính chất lý hóa

Tính chất vật lý
- Trạng thái và màu sắc: Ở dạng khan, axit phosphoric là chất rắn tinh thể trong suốt, không màu. Dạng dung dịch phổ biến là chất lỏng sánh, trong suốt, không màu.
- Mùi vị: Không mùi, có vị chua.
- Độ tan: Tan vô hạn trong nước và etanol.
- Nhiệt độ nóng chảy: 42.35 °C (dạng khan H₃PO₄). Dạng ngậm nước H₃PO₄.H₂O có nhiệt độ nóng chảy 29.32 °C.
- Nhiệt độ phân hủy/sôi: Bắt đầu mất nước và phân hủy ở khoảng 213 °C để tạo thành các axit polyphotphoric như axit pyrophosphoric (H₄P₂O₇) và axit metaphosphoric (HPO₃) ở nhiệt độ cao hơn (260-300 °C).
- Tỷ trọng: Khoảng 1.87 g/cm³ (dạng rắn) hoặc 1.88 g/cm³ (dung dịch 85%).
Tính chất hóa học
-
Tính axit: Axit phosphoric là một axit ba nấc có độ mạnh trung bình. Trong dung dịch, nó phân ly thuận nghịch theo ba nấc, chủ yếu là nấc đầu tiên:
- H₃PO₄ ⇌ H⁺ + H₂PO₄⁻ (Ka1 ≈ 7.1 x 10⁻³ đến 7.6 x 10⁻³)
- H₂PO₄⁻ ⇌ H⁺ + HPO₄²⁻ (Ka2 ≈ 6.2 x 10⁻⁸ đến 8 x 10⁻⁶)
- HPO₄²⁻ ⇌ H⁺ + PO₄³⁻ (Ka3 ≈ 4.2 x 10⁻¹³ đến 4 x 10⁻¹³)
- Dung dịch axit phosphoric làm quỳ tím chuyển sang màu đỏ.
- Tác dụng với oxit bazơ tạo thành muối và nước.
- Tác dụng với bazơ tạo thành muối và nước, tùy thuộc vào tỷ lệ phản ứng có thể tạo ra muối dihydrogen phosphate, hydrogen phosphate hoặc phosphate.
- Tác dụng với kim loại đứng trước hydro trong dãy hoạt động hóa học để tạo thành muối photphat và giải phóng khí hydro (H₂).
- Có thể phản ứng với một số muối để tạo thành axit mới và muối photphat mới.
-
Tính oxi hóa/khử: Trong phân tử H₃PO₄, photpho ở mức oxi hóa +5 là mức oxi hóa cao nhất và bền. Do đó, axit phosphoric khó bị khử và không có tính oxi hóa mạnh như axit nitric (HNO₃) ở nhiệt độ thường. Nó không có tính khử.
-
Phản ứng nhiệt phân: Khi đun nóng đến nhiệt độ cao, axit phosphoric mất nước tạo thành các axit polyphotphoric:
- Ở 200-250 °C: 2H₃PO₄ → H₄P₂O₇ + H₂O (axit pyrophosphoric).
- Ở 300-500 °C: H₄P₂O₇ → 2HPO₃ + H₂O (axit metaphosphoric).